Výzkumná skupina Bioorganické chemie a biomateriálů z ÚCHP AV ČR vedla mezioborový výzkumný tým, který vyvinul novou třídu inhibitorů lidského galektinu-1 založených na organorutheniových komplexech. Výsledky byly publikovány v časopise Journal of Medicinal Chemistry.
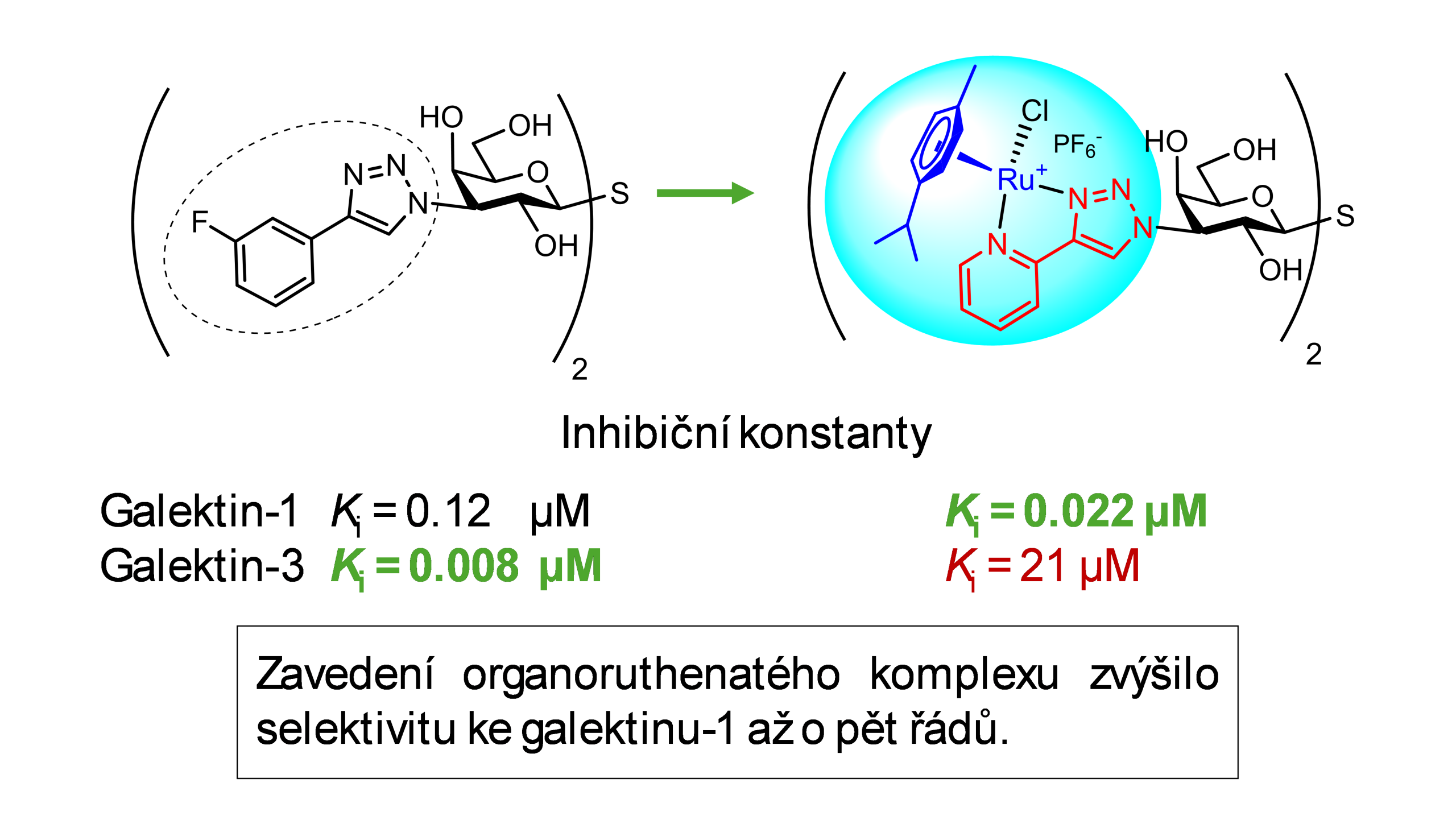
Galektin-1 je protein interagující s některými sacharidy na buněčném povrchu, který hraje významnou roli v regulaci imunitní odpovědi a nádorového mikroprostředí. Zvýšená aktivita tohoto proteinu může podporovat růst nádorů a potlačovat protinádorovou imunitu, což z něj činí atraktivní cíl pro vývoj nových léčiv. Vývoj selektivních inhibitorů je však obtížný, protože vazebná místa jednotlivých galektinů jsou si strukturně velmi podobná. Výzkumný tým proto navrhl nové inhibitory založené na disacharidu thiodigalaktosidu, který byl modifikován organorutheniovým arénovým komplexem. Tato neobvyklá kombinace sacharidové chemie a organokovových struktur vedla ke vzniku látek s nanomolární afinitou a mimořádně vysokou selektivitou ke galektinu-1 – afinita ke galektinu-1 je až tři řády vyšší ve srovnání s afinitou k příbuznému galektinu-3.
Nejúčinnější sloučeniny byly schopny blokovat vazbu galektinu-1 na povrch nádorových buněk a zastavit galektinem-1 indukovanou deaktivaci T-lymfocytů. Tyto výsledky ukazují, že organorutheniové glykomimetické struktury představují slibnou strategii pro vývoj selektivních inhibitorů galektinů s potenciálním využitím v protinádorové terapii.
Na výzkumu se též podíleli vědci z Masarykova onkologického ústavu, Biofyzikálního ústavu AV ČR, Ústavu organické chemie a biochemie AV ČR a Mikrobiologického ústavu AV ČR.
- Hamala V., Kurfiřt M., Červenková Šťastná L., Dvořák F., Bernášková J., Sýkorová A., Kozák J., Zavřel M., Staroňová T., Šebest P., Ostatná V., Červený J., Bojarová P., Holčáková J., Hrstka T., Hrstka R., Karban J.: Organoruthenium Glycomimetics Exhibit High Selectivity and Nanomolar Affinity for Human Galectin 1. J. Med. Chem. 2026, 69(4), 4789-4809. doi.org/10.1021/acs.jmedchem.5c03436